
As campanhas dos chamados “meses coloridos” surgiram, e se mantêm vivas no imaginário popular com o seguinte ideal: é sempre melhor prevenir do que remediar. O setembro amarelo chama a atenção para o suicídio, lembrando a população de se atentar a sinais depressivos de colegas e de parentes. O Outubro Rosa, talvez o mais emblemático, alerta para o câncer de mama (já discutimos ano passado nessa live!).
Finalmente chegamos no Novembro Azul, que preconiza o RASTREAMENTO (screening) do câncer de próstata, com o seguinte racional: o CA Próstata é um câncer bem prevalente, que mata muitos homens. Quanto mais cedo identificamos um câncer, menor ele vai estar e mais fácil será o tratamento para cura. Então a conclusão é óbvia! Já que temos exames, toque retal e PSA sérico, que “detectam” o CA próstata, quanto mais cedo fizermos nos homens, mais cedo encontramos o tumor, mais cedo tratamos e salvamos muitas vidas! No entanto, é bem raro que as mensagens desses períodos do ano sejam balanceadas, informando o que pacientes ou até mesmo clínicos precisam saber. Em geral, vemos um exagero dos benefícios, além da ausência da discussão dos danos. [1]
Quer entender do assunto e enterrar de vez essa polêmica? Então vamos nessa!
Dando nome aos bois…
É sempre bom lembrarmos: Rastreamento é a procura de uma doença (ou fator de risco) em pessoas sem sintomas da doença sendo rastreada. Rastreamento não envolve apenas um único teste ou exame, mas toda a sequência de eventos necessária para atingir a desejada redução de risco.
O que rastreamento não é: ir ao médico ou fazer exames por ter percebido o aparecimento de algum sintoma de câncer de próstata. Esses sintomas podem ser: hematúria (sangue na urina), polaciúria (aumento da frequência, com eliminação de pouco líquido), urgência (ter que “sair correndo” para o banheiro), jato fraco ou interrompido, esforço miccional (fazer muita força para conseguir urinar), incontinência urinária (liberação da urina de maneira involuntária), noctúria (aumento idas ao banheiro à noite) ou dor suprapúbica (na região inferior do abdome). Nesses casos, há uma suspeita diagnóstica, que então leva à realização dos exames de toque retal, PSA sérico, tomografias, entre outros.
Então, vamos deixar bem claro: neste texto, estamos tratando do rastreamento, ou seja, o paciente está assintomático (vulgo, “não tem nada”), e mesmo assim vai ao médico para realização de exames de “check-up” ou de rotina para o câncer de próstata.
Será que essa prática é realmente tão boa? Ou, para falar português claro: será que ela tem algum benefício real? Ou, pior: será que ela não pode ser danosa ao paciente?
Screening, quais os requisitos?
Definido o nosso alvo, o screening de câncer de próstata, precisamos entender quais as ponderações necessárias em qualquer programa de rastreamento. Inicialmente, partimos de um grupo populacional muito amplo (todos os homens dentro de uma faixa etária), sendo que há naturalmente uma baixa probabilidade INDIVIDUAL para desenvolvimento de câncer de próstata (e probabilidade ainda menor de morte por esse câncer), assim como para qualquer doença.
O segundo ponto foi melhor resumido por Stanley O. Hoerr: “É difícil fazer um paciente assintomático se sentir melhor”. Logo, qualquer intervenção já parte do ponto alto da saúde do indivíduo, com um grande potencial de dano. Assim, é mais fácil piorar a qualidade de vida de alguém sem sintomas, do que melhorá-la.
O terceiro ponto, na verdade, são vários. A OMS (Organização Mundial da Saúde) preconiza alguns princípios básicos para realização de qualquer programa de rastreamento populacional, sendo alguns deles:
(1) A doença é um problema de saúde importante?
→ Sim, é o segundo tumor mais prevalente nos homens.
(2) Há tratamento (melhor quando precoce, do que com sintomas)?
→ Sim, inclusive são bem invasivos, como quimioterapia, radioterapia e cirurgia, que trazem efeitos colaterais que diminuem, em muito, a qualidade de vida.
(3) Há exames para diagnóstico na fase pré-clínica e tratamento?
→ Sim, o exame de toque e PSA são simples e amplamente disponíveis. Por outro lado, poucos se lembram que a investigação não se encerra neles, sendo o próximo passo as biópsias e cirurgias, as quais não são isentas de risco (ansiedade de ter o diagnóstico de câncer, hemorragias, infecções, incontinência urinária e impotência sexual).
(4) Possui estágio latente e com história natural bem compreendida?
→ Sim, mas é latente até demais. A maioria dos tumores de próstata cresce de maneira tão lenta, que não chega a causar sintomas ou provocar metástases, ou seja, não causa danos à saúde do paciente. Na maior parte dos casos, o paciente morre com o câncer de próstata, e não por causa dele.
Aqui entram outras duas informações interessantes que enviesam as estatísticas de sobrevida nas pesquisas de rastreamento, os vieses do “tempo de antecipação do diagnóstico” e do “tempo de duração”.
No viés de antecipação do diagnóstico [2], o rastreamento detecta um caso antes do que ele se apresentaria naturalmente, mas não altera o prognóstico. Isso cria a falsa percepção que o paciente viveu mais tempo após o diagnóstico, mas na verdade só o que aconteceu foi a antecipação da data do diagnóstico, sem mudança da história natural da doença. Em outras palavras, a data da morte continuou a mesma.
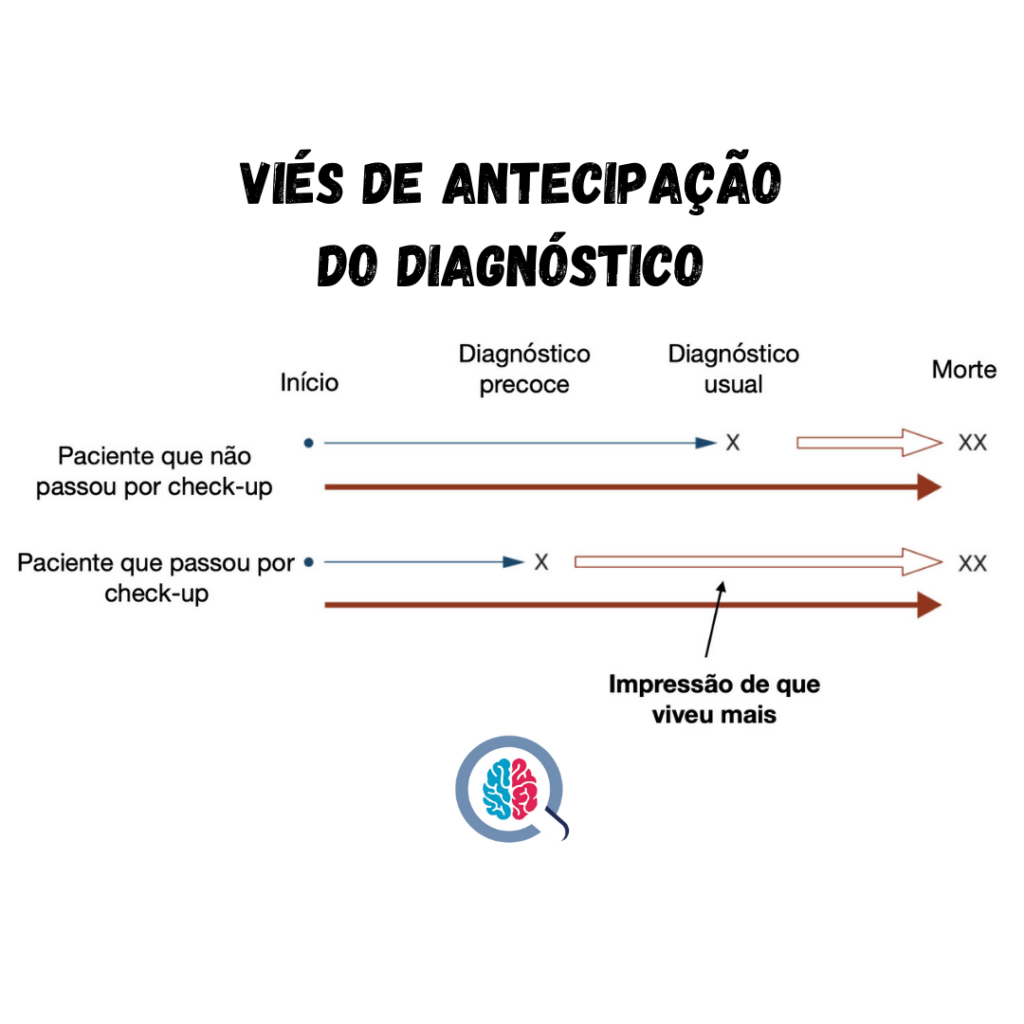
Figura 1: Adaptado: https://twitter.com/josenalencar/status/1342838168593330176
Aqui, cabe comentar uma característica dos cânceres que é muito pouco falada: o câncer é uma doença com comportamento muito heterogêneo. Isso significa que um mesmo câncer não se desenvolve de maneira linear em todos os pacientes, isto é, nem todos crescem em ritmo constante, o que permitiria sempre a detecção precoce, seguido de um tratamento totalmente resolutivo, levando à queda da mortalidade. E isso nos leva a outro viés!
No viés de tempo de duração [2], há mais chances do screening identificar uma doença lenta e progressiva do que uma rápida e fulminante. Isso coloca os casos que naturalmente já teriam um prognóstico melhor (os de crescimento lento) entre aqueles detectados por rastreamento. Já os casos de pior prognóstico continuarão sendo diagnosticados como sempre foram: pelo surgimento de sinais e sintomas associados ao seu crescimento rápido. Assim, aumenta-se o denominador das doenças e o numerador de sobreviventes dos pacientes rastreados, inflando artificialmente a sobrevida.
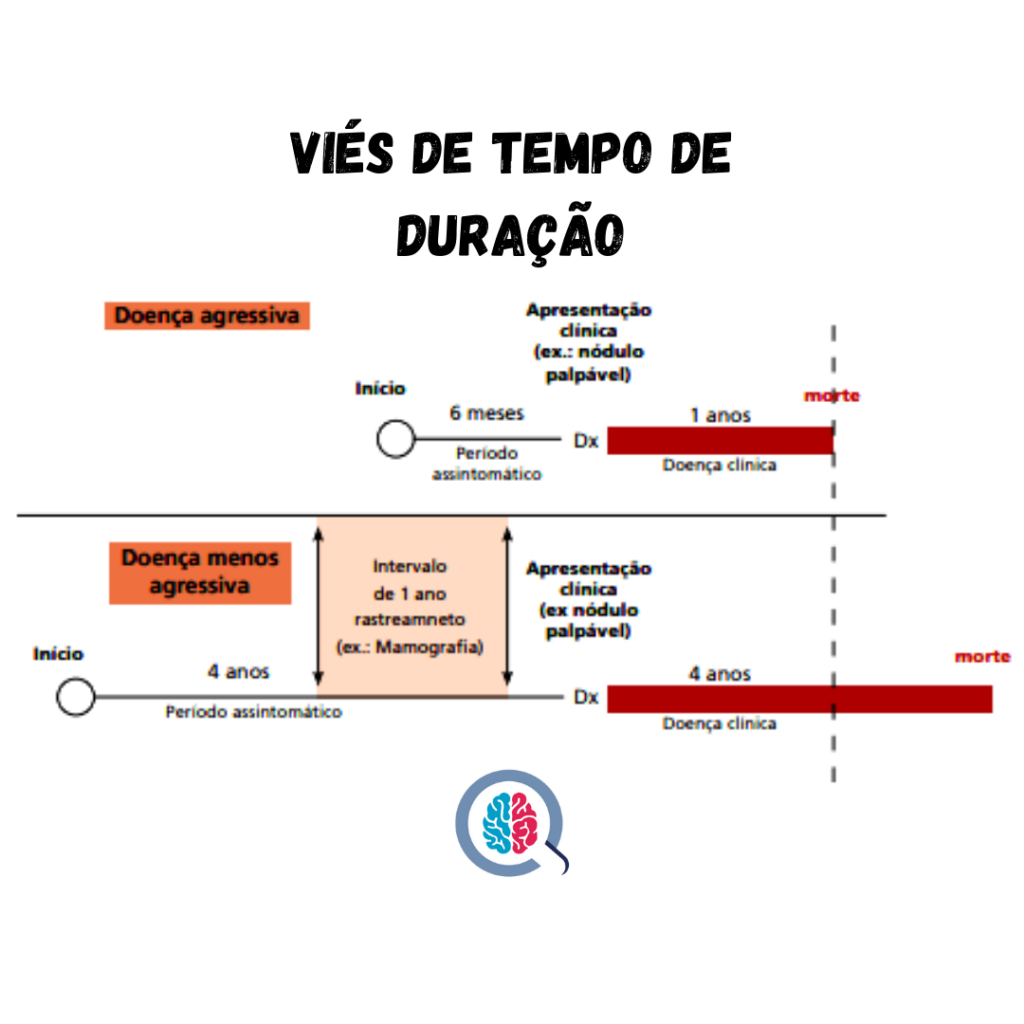
Figura 2: Adaptado: Brasil. Ministério da Saúde. Secretaria de Atenção à Saúde. Departamento de Atenção Básica. Rastreamento / Ministério da Saúde, Secretaria de Atenção à Saúde, Departamento de Atenção Básica. Brasília: Ministério da Saúde, 2010. Pág 27.
Uma analogia útil é do celeiro, popularizada pelo especialista em rastreamento de câncer, Dr. H. Gilbert Welch [3]. Imagine a seguinte situação: você quer evitar que os animais de sua fazenda escapem, construindo para isso uma cerca em tempo hábil. Na fazenda, existem pássaros, coelhos e tartarugas.
Os pássaros vão fugir, apesar da construção de qualquer cerca. Esses simbolizam os cânceres de crescimento rápido e com maiores taxas de metástases. Apesar de serem os mais letais, o rastreamento não consegue ajudar nesses casos. Isso ocorre porque eles tendem a crescer e causar sintomas no intervalo entre um exame de rastreamento e o próximo. Ou seja, até a data do próximo exame, eles já “escaparam” e inevitavelmente causarão a morte do paciente.
Os coelhos conseguem ser capturados até a construção da cerca, porém conseguem escapar sem elas. Esse animal representa os tumores passíveis de detecção precoce e que causariam danos ao paciente. Logo, a detecção precoce (pelo rastreamento) pode ajudar nesse caso em específico, contanto que o tratamento precoce (na fase assintomática) seja melhor do que o tratamento dado após o aparecimento dos sintomas.
As tartarugas são cânceres de crescimento tão lento, e com risco de metástases tão baixo, que nem precisamos das cercas, pois elas não vão a lugar algum. Neste caso, o rastreamento só vai identificar um tumor indolente, que pode conviver com o paciente por muitos anos sem gerar dano algum. Em alguns casos, os tumores podem até regredir sozinhos (já existem mecanismos fisiopatológicos que buscam explicar isso [4]). Este pode ser um conceito totalmente novo para alguns dos nossos leitores, pois somos bombardeados desde muito cedo com a ideia que o câncer é a doença mais maligna e letal que existe. E, adivinha? O câncer de próstata é um exemplo onde podemos encontrar muitas tartarugas.
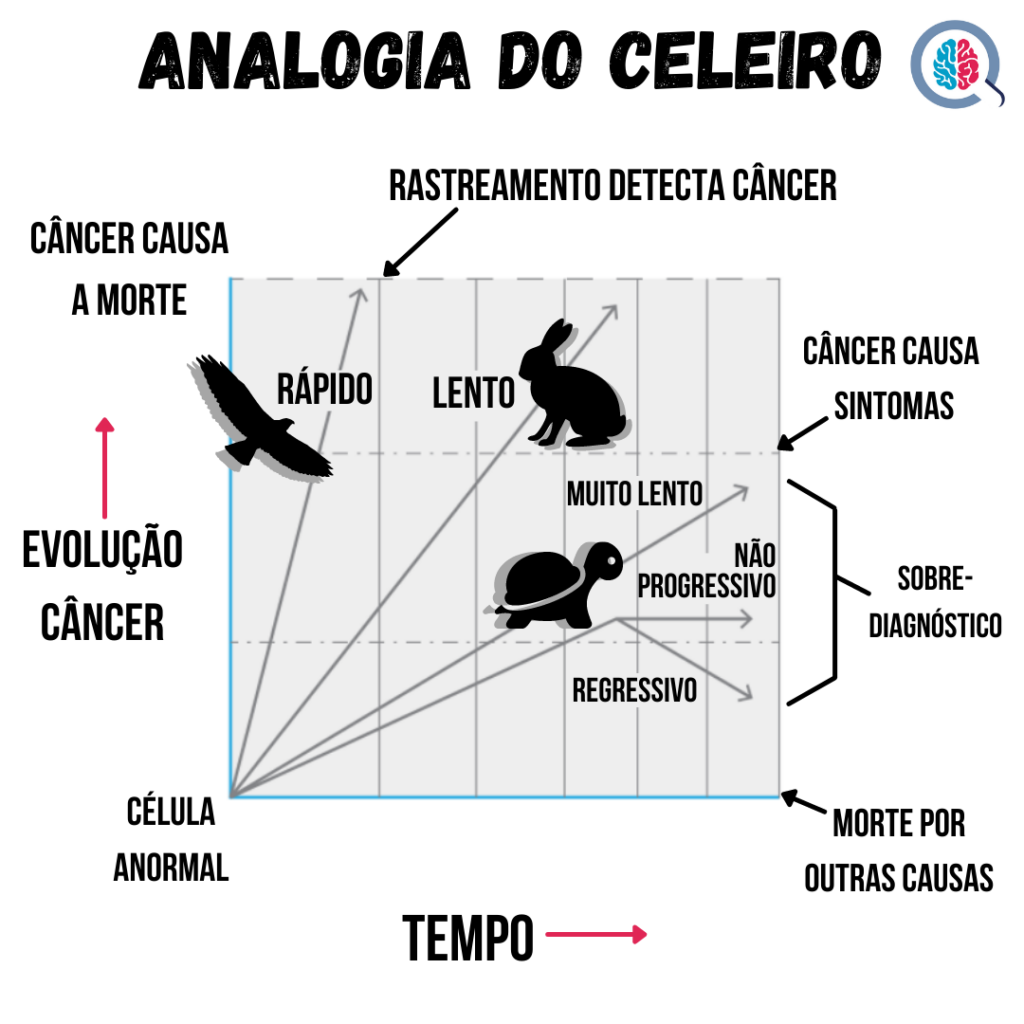
Figura 3 – Progressão heterogênea do câncer e a analogia do celeiro. Adaptado de [4].
Agora, você deve estar se perguntando: qual o problema de fazer uma cerca para as tartarugas? Não é melhor “pecar por excesso”? Na pior das hipóteses só gastamos mais recursos desnecessariamente – certo?
Errado! Quando identificamos doenças que não teriam repercussão clínica, ou seja, não causariam qualquer prejuízo à sobrevida ou à qualidade de vida de um indivíduo, estamos realizando um sobrediagnóstico (em inglês, overdiagnosis) [5]. Veja, isso não significa um diagnóstico errado ou um falso-positivo. Se a biópsia mostra que o paciente tem câncer de próstata, isso geralmente significa que existem, sim, células cancerosas naquele paciente. O problema é que muitas vezes esse câncer iria se comportar de forma inofensiva, com crescimento muito lento ou sem crescimento algum! Este paciente iria morrer COM o câncer de próstata, muitos anos depois, e não DO câncer.
E a história não para por aqui! Quando um médico encontra uma doença, ele não a trata? Claro que sim! Ainda mais se o nome da doença começar com “câncer”. Contudo, lembre que o câncer desse paciente é um sobrediagnóstico, um diagnóstico que não deveria ter ocorrido e só ocorreu porque o paciente foi rastreado.
Logo, a consequência desse rastreamento é o sobretratatamento (em inglês, overtreatment) [4] [5], que consiste no uso de terapias (cirurgia, radioterapia, quimioterapia) em um indivíduo assintomático, que não tem como melhorar! Como qualquer intervenção tem riscos potenciais de dano, se a realizarmos em alguém que não terá qualquer benefício, só sobrarão os malefícios desse tratamento: impotência sexual, incontinência urinária, queda de cabelo, fraqueza, gastos com viagens e consultas, sem falar na carga de ser “rotulado” como um doente de câncer, trazendo todos os prejuízos financeiros, empregatícios, familiares e psicológicos que esse rótulo acarreta.
O ponto mais importante, que poderia suplantar todos os demais levantados, é: há realmente evidências robustas que respaldam o rastreamento do câncer de próstata em homens assintomáticos? O benefício que é vendido pelo novembro azul (a redução de mortalidade pelo câncer de próstata com o rastreamento) é verdadeira?
O que dizem as evidências (há mais benefício que malefício)?
De acordo com a revisão da USPSTF [6] (United States Preventive Services Task Force) de 2018, dois estudos randomizados controlados de melhor qualidade nos informam sobre os possíveis benefícios e malefícios do rastreamento do câncer de próstata: PCLO e ERSPC.
O PLCO, apesar de ter detectado mais cânceres de próstata no grupo rastreado em comparação com o controle, não mostrou redução da mortalidade do câncer de próstata. Portanto, esse estudo contesta uma das grandes afirmações do Novembro Azul: a de que “o rastreamento do câncer de próstata salva vidas”.
Esse estudo, entretanto, sofreu do viés de contaminação: boa parte do grupo controle foi exposto ao rastreamento em algum momento. Ou seja, os resultados foram enviesados contra o rastreamento. Por conta disso, esse estudo passou a ser considerado como uma comparação entre rastreamento sistemático versus oportunístico.
Já o ERSPC rastreou homens entre 55-69 anos a cada 4 anos (ou a cada 2 anos, na Suécia) e teve um acompanhamento de 13 anos. O PSA (antígeno prostático específico) foi utilizado como o principal exame de rastreamento. Alguns centros do estudo utilizaram exames adicionais de rastreamento, como toque retal e ultrassonografia transretal.
Com esse estudo, a primeira pergunta que devemos fazer é: quantas mortes o rastreamento poderia evitar? Para isso, precisamos olhar para o grupo controle. Imagine um teatro lotado com 1000 homens. No final do acompanhamento de 13 anos, desses 1000 homens, 6 morreram de câncer de próstata. Dessa forma, é impossível que o rastreamento evite mais do que 6 mortes a cada 1000 homens rastreados por 13 anos. Isso é muitas vezes não compreendido por pacientes, que frequentemente superestimam os benefícios do rastreamento, especialmente quando a redução da mortalidade é apresentada como redução do risco relativo.
Qual, então, o benefício apontado pelo ERSPC? De 1000 homens rastreados, 1 morte de câncer de próstata foi evitada e 3 casos metastáticos foram evitados. Para isso, foi necessário diagnosticar e tratar 27 homens. Isso quer dizer que 24 homens foram diagnosticados e tratados (com uma combinação de cirurgia, quimioterapia e hormonioterapia) de forma desnecessária. Esse é o dano mais sério do rastreamento: o sobrediagnóstico, e sua consequência, o sobretratamento.
A USPSTF fez estimativas dos riscos baseados no ERSPC e outros estudos, trazendo informações que ilustram as consequências quando 1000 homens foram rastreados por vários anos: 240 falsos-positivos, 220 biópsias desnecessárias, 65 cirurgias de prostatectomia radical (retirada da próstata) ou radioterapia, 50 homens que ficaram com impotência sexual, 15 que ficaram com incontinência urinária e 5 que morreram apesar do rastreamento.

Figura 4 – Descrição visual do efeito do rastreamento de câncer de próstata, em 1000 homens.
Periodicidade, faixa etária e outros exames de rastreamento
As campanhas raramente mencionam qualquer dano por conta do rastreamento. Por não perceberem os danos, como sobrediagnóstico, sobretratamento e procedimentos desnecessários, as campanhas sugerem a realização de rastreamento anualmente, começando aos 40 anos. No ERSPC, a redução da mortalidade do câncer de próstata apareceu na faixa etária de 55 a 69 anos. Além disso, a periodicidade principal no estudo foi de 4 anos.
Por acreditar que o rastreamento do câncer de próstata causa mais malefícios do que os possíveis benefícios, o INCA não recomenda o rastreamento rotineiro do câncer de próstata.
Só como outro exemplo, considere o rastreamento do câncer de mama com mamografia. Neste caso, a recomendação do INCA é que seja realizado para a faixa etária entre 50 e 69 anos, a cada dois anos. Mesmo com essa recomendação explícita, as matérias publicadas na mídia durante o Outubro Rosa fazem recomendações equivocadas quanto à faixa etária e à periodicidade do rastreamento, além de sugerirem exames ou práticas não recomendadas [7].
É importante entendermos que o rastreamento em excesso não solucionará o problema do câncer de próstata, mas apenas gerará mais falsos-positivos, sobrediagnóstico e sobretratamento. Estudos mostram que o rastreamento causa o paradoxo da popularidade: quanto mais sobrediagnóstico o rastreamento causa, mais pessoas acreditam que suas vidas foram salvas [2]. No caso do câncer de próstata, sabemos que o rastreamento oportunístico tem menos chance de oferecer benefício do que aquele visto no ERSPC ou em um programa organizado. No rastreamento oportunístico, a eficácia reportada é menor, quase duplicando o número de homens necessários para rastrear, além de aumentar o número de sobrediagnósticos [8].
Outro detalhe interessante é que a maioria dos estudos se baseia no PSA como principal exame de rastreamento. Outros exames adicionais às vezes foram utilizados, como é o caso do toque retal ou até a ultrassonografia transretal (TRUS), utilizada em alguns centros do ERSPC. Entretanto, entendemos que as campanhas colocam um destaque maior ao exame de toque, culturalmente observado na população leiga e largamente encontrada em programas de humor, sem mencionar que o principal é o PSA.
O que significa salvar vidas?
Você deve ter percebido que, até o momento, falamos sempre da redução da mortalidade do câncer de próstata. O PLCO e ERSPC utilizaram a mortalidade do câncer de próstata como desfecho principal. No entanto, a utilização desse desfecho parte do pressuposto que a causa da morte pode ser identificada corretamente.
Dois vieses importantes podem ocorrer na mortalidade específica da doença. O viés slippery linkage to screening (em tradução livre, viés de vazamento relacionado ao rastreio) ocorre porque mortes por outras causas em pacientes rastreados não são atribuídas à mortalidade específica da doença [9]. Lembre-se que há muito mais pacientes com diagnósticos e tratamentos desnecessários do que mortes de câncer de próstata evitadas. A ideia é que mortes podem ocorrer por conta do rastreamento (por exemplo, por complicações de cirurgia ou radioterapia), sendo essas mortes atribuídas a outras causas (e não “morte por câncer de próstata”). Dessa forma, reduz-se a morte do câncer rastreado, mas pode aumentar (na mesma quantidade ou até mais) mortes por outras causas, pendendo a balança para mortes fora do rastreamento. Por esse motivo, esse viés favorece o rastreamento.
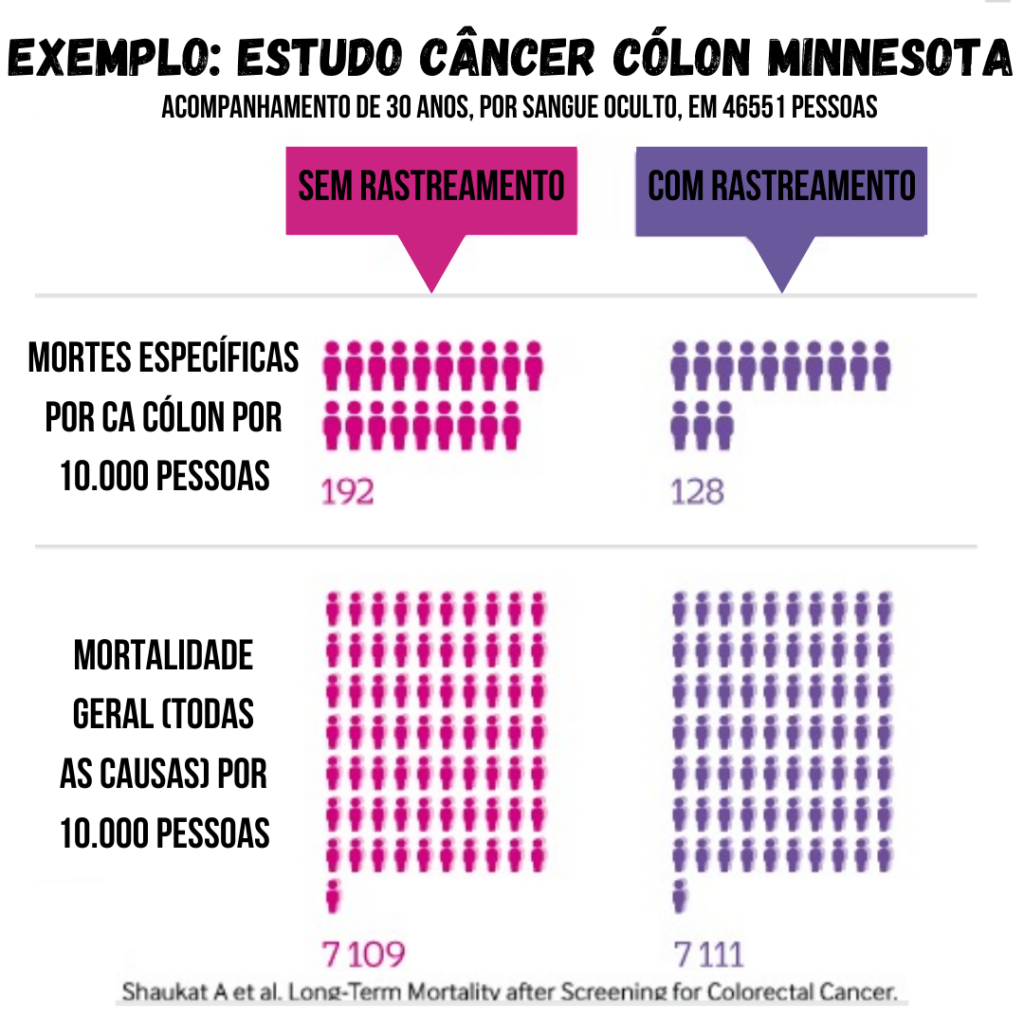
Figura 5 – Desfechos de mortalidade do câncer rastreado em comparação com a mortalidade geral no estudo de Minnesota (rastreamento de câncer colorretal). Adaptado de [10]
O segundo viés, chamado de sticky diagnosis from screening (em tradução livre, diagnósticos aderidos ao rastreamento), ocorre quando mortes por outras causas em pacientes rastreados,devido a erros de julgamento, são erroneamente atribuídas à doença rastreada [9]. Esse viés desfavorece o rastreamento.
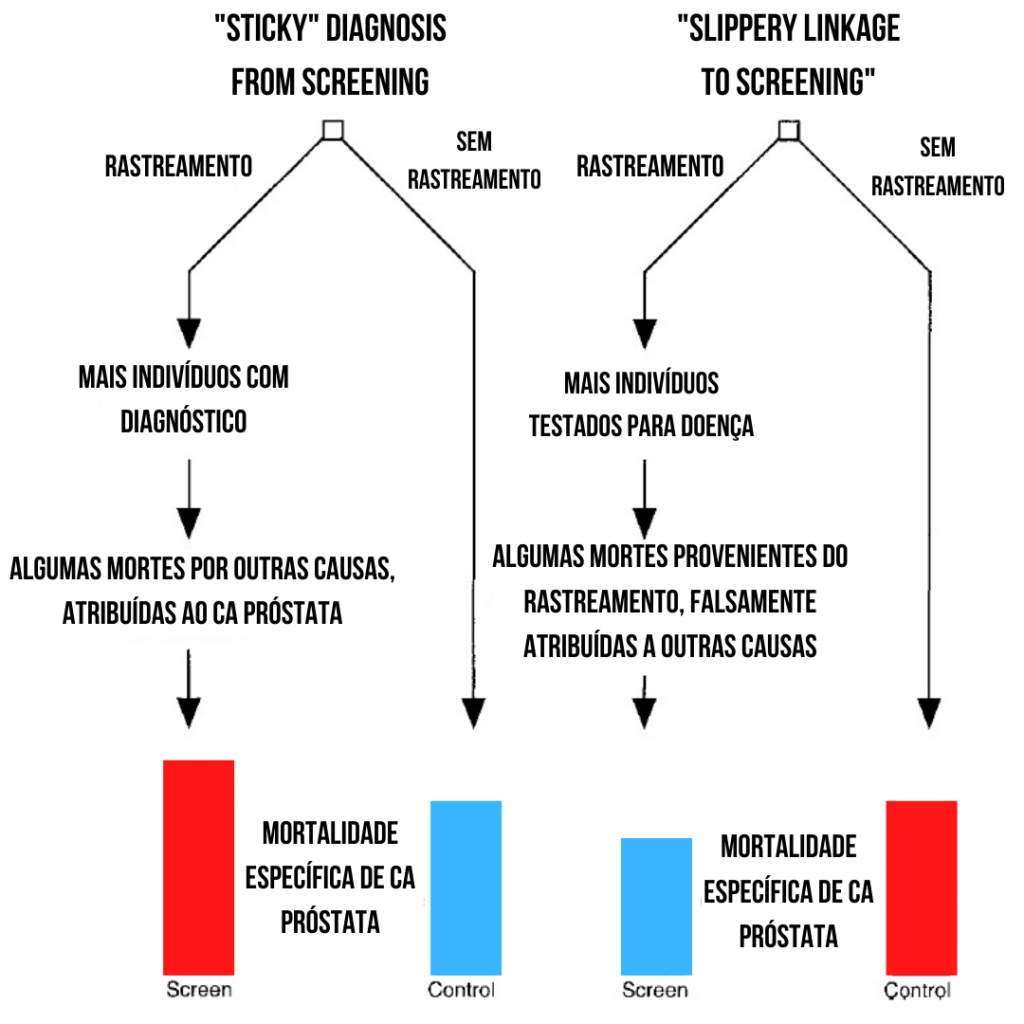
Figura 6 – Os vieses da mortalidade específica da doença. Adaptado de [9]
Em outras palavras, até mesmo os estudos feitos para pesquisa podem não ser desenhados da melhor forma, com mortes provenientes do rastreamento “vazando” e sendo classificadas como não relacionadas ao câncer, levando ao “benefício imaginário” do rastreamento (já que não foram consideradas consequência deste) ou, se consideradas como relacionadas ao rastreamento, aumentar muito as mortes específicas e desfavorecer artificialmente o rastreamento.
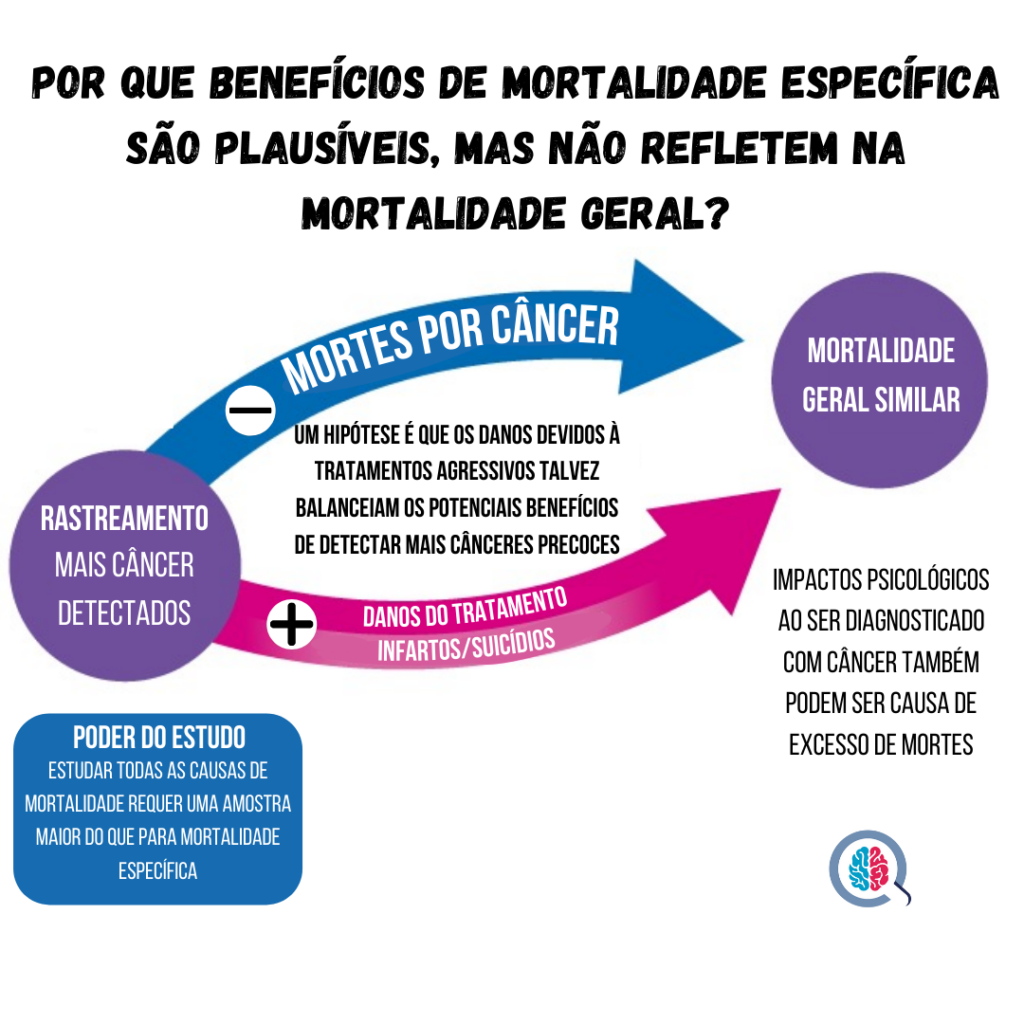
Figura 7 – Motivos para a redução da mortalidade específica não refletir na mortalidade geral. Adaptado de [10].
A mortalidade geral é o desfecho, que evita ambos vieses. Como os estudos de rastreamento não mostraram redução da mortalidade geral, logo, podemos dizer que o principal objetivo de salvar vidas não foi ainda demonstrado. Geralmente, a amostra necessária para detectar qualquer diferença na mortalidade geral é muito grande. Isso nos mostra que qualquer benefício na mortalidade geral será muito pequeno. No seu livro “Less Medicine, More Health”, o Dr. H. Gilbert Welch deixa isso bem claro: “devemos abandonar a linguagem de que o rastreamento salva vidas. Devemos reconhecer publicamente que não sabemos se a detecção precoce aumenta, encurta ou não tem nenhum impacto na duração da vida das pessoas. E devemos ser claros que, se precisamos de muitas pessoas para descobrir com certeza, então, o benefício será, no melhor dos casos, muito pequeno.
Em 2011, o BMJ publicou um debate a respeito de qual seria o melhor desfecho para julgar programas de rastreamento de câncer [11] [12].
E agora? O que fazemos com essas informações?
Se você é um paciente que passa constantemente por tais exames, o primeiro passo é compreender qual o alvo desse texto: o rastreamento, ou seja, testar pessoas assintomáticas para o câncer de próstata. Se o seu médico recomendar PSA com ou sem toque retal, converse com ele sobre quais os benefícios e danos para você entender qual a real necessidade da realização desses exames.
Por outro lado, com ou sem rastreamento, caso você tenha quaisquer sintomas urinários, procure o urologista, que saberá conduzir o processo diagnóstico. Aqui, assim como faz o INCA, precisamos diferenciar o rastreamento do diagnóstico precoce. Pode ocorrer uma confusão dado que o objetivo do rastreamento é a detecção precoce através da realização de exames em pessoas sem sintomas. Já o diagnóstico precoce é o reconhecimento imediato dos primeiros sinais e sintomas, para que o diagnóstico possa ser feito o quanto antes.
Se você é um profissional da saúde que não recomenda screening, alerte os pacientes sobre o diagnóstico precoce por meio dos sintomas urinários e eduque-os para os riscos envolvidos na prática do rastreamento (você pode baixar as imagens deste texto e usar como ilustração nas suas conversas).
Se você é um médico que realiza ou recomenda screening de câncer de próstata em seus pacientes, sua primeira ação deve ser se informar (veja as referências bibliográficas abaixo e tire suas próprias conclusões) e, depois, repensar suas práticas. A USPSTF sugere que a decisão de rastrear ou não o câncer de próstata seja compartilhada entre médico e paciente. O screening de câncer de próstata atenta contra 2 de nossos pilares éticos: a beneficência (não há redução de mortalidade geral; a redução da mortalidade específica do câncer ainda é discutível) e a não-maleficência (geram-se muitos danos, que superam qualquer possível benefício).
Conclusões:
O Novembro Azul é um caso clássico de “Medical Reversal” [13], quando práticas médicas enraizadas acabam por se demonstrarem sem fundamento, ou pior, mais maléficas que benéficas. Isso nos traz à reflexão sobre o papel do médico como promotor de saúde, sendo que na maioria das vezes “mais nem sempre é melhor”.
Práticas que parecem hoje absurdas foram o padrão em eras passadas. Quantos homens no passado não morreram por causa da sangria? O próprio George Washington, um ex-presidente estadunidense, foi vítima dessa prática!
Indivíduos bem intencionados e desprovidos das melhores evidências, talvez, sejam os mais responsáveis por danos não intencionais. Como exemplo, o grupo de escoteiros Eclaireurs de France, que limpava pichações em uma caverna no interior da França, recebeu o prêmio satírico “Ig Nobel” na seção arqueologia [14]. Por que? As pichações na realidade eram pinturas rupestres. Informações ruins, recheadas de boas intenções.
Vale lembrar que as conclusões deste texto são semelhantes às de outras entidades de renome nacional e internacional, como a Choosing Wisely [15], a Choosing Wisely Brasil [16], a USPSTF [6], a American Society of Clinical Oncology [17] e a American Academy of Family Physicians [18], INCA [19].
Diante de todo o exposto, podemos tirar algumas conclusões:
- A campanha Novembro Azul superestima os benefícios e omite os danos potenciais do rastreamento de câncer de próstata.
- O screening do câncer de próstata traz muitos malefícios (ansiedade, custo, falsos-positivos, biópsias desnecessárias, sobrediagnóstico e sobretratamento).
- Desfechos negativos não são evitados na maioria dos tumores pela detecção precoce, devido aos casos de evolução muito rápida e letal (os “pássaros”) .
- Cuidado com suas boas intenções! Elas podem não ser suficientes (e podem até ser deletérias!) na ausência de evidências de benefício.
Autores:

Alexandre Bissoli é acadêmico de medicina do 5º período, na Universidade Estadual de Londrina, editor júnior do site Raciocínio Clínico, membro do projeto STARS-CWB e entusiasta de medicina baseada em evidências e baseada em valor, sempre em busca do melhor caminho.

Felipe Nogueira é Doutor em ciências médicas pela UERJ, além de Mestre e Bacharel em informática pela PUC-Rio. Tem escrito em diversas mídias sobre as complexidades do rastreamento do câncer desde 2019. Divulgador da ciência e do pensamento crítico com artigos publicados nas revistas Skeptical Inquirer, Skeptic e no seu blog Ceticismo e Ciência.
PARA SABER MAIS:
[1] Nada é azul na campanha do “Novembro Azul” | Questão de Ciência (revistaquestaodeciencia.com.br)
[2] Screening: Evidence and Practice
[3] The heterogeneity of cancer | SpringerLink
[4] Overdiagnosis in Cancer | JNCI: Journal of the National Cancer Institute | Oxford Academic (oup.com)
[5] What is overdiagnosis and why should we take it seriously in cancer screening? | PHRP
[7] Detecção precoce do câncer de mama na mídia brasileira no Outubro Rosa
[10] Why cancer screening has never been shown to “save lives”—and what we can do about it | The BMJ
[13] Ending Medical Reversal | Johns Hopkins University Press Books (jhu.edu)
[14] State Acts Against Do-Gooders Who Destroyed Ancient Cave Drawings (apnews.com)
[15] Search Recommendations | Choosing Wisely
Outras referências:
Mitos nas campanhas de prevenção de câncer | Questão de Ciência (revistaquestaodeciencia.com.br)
Capítulo 12 – Rastreamento de Câncer Baseado em Evidências (autores: Felipe Nogueira e Arn Migoswki) do livro Manual de Medicina Baseada em Evidências (autor: José Alencar, editora Sanar)
Detecção precoce do câncer / Instituto Nacional de Câncer José Alencar Gomes da Silva




A divulgação desse tipo de pensamento é de extrema importância no meio médico e entre a população geral. Parabéns pelo conteúdo e principalmente por disseminar o pensamento médico racional e baseado em evidências.